骨質(zhì)疏松癥(OP)是一種以骨量降低、骨組織微結(jié)構(gòu)破壞,導(dǎo)致骨脆性增加、骨強(qiáng)度下降,易發(fā)生骨折為特征的全身性代謝骨病。骨質(zhì)疏松癥已被世界衛(wèi)生組織列為僅次于心血管疾病的第二大危害人類健康的疾病,被稱為“沉默的殺手”。相關(guān)研究報(bào)告顯示,中國(guó)是世界上骨質(zhì)疏松癥患者最多的國(guó)家,約有9000萬(wàn)人罹患此病,其發(fā)病率與年齡息息相關(guān)。OP的危害主要為易發(fā)骨折、骨質(zhì)疏松性骨折導(dǎo)致的殘疾、心肺功能障礙等,極大地影響老年人生活質(zhì)量。
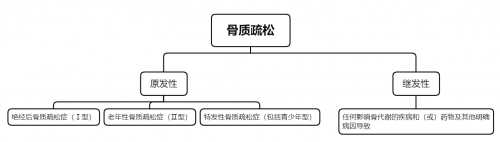
圖1. OP的分類
動(dòng)物模型選擇選擇與骨質(zhì)疏松癥(OP)的分類
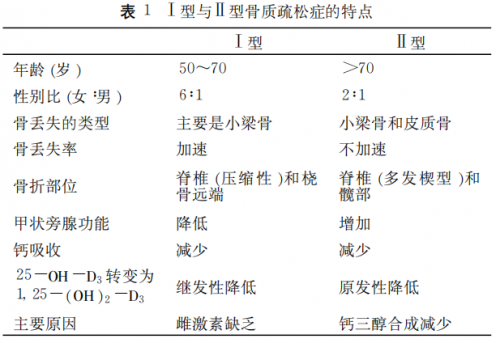
OP發(fā)病受多重因素影響,包括遺傳、激素、營(yíng)養(yǎng)、年齡、生活習(xí)慣及免疫學(xué)等。臨床常見的OP根據(jù)病因可分為原發(fā)性、繼發(fā)性兩大類[1]。而原發(fā)性O(shè)P是臨床最常見的類型(約占80%),又分為 Ⅰ 型高轉(zhuǎn)換型OP(以骨吸收增加為主,常見于絕經(jīng)后女性)、Ⅱ 型低轉(zhuǎn)換型OP(以骨形成減少為主,常見于老年人)以及特發(fā)性O(shè)P(包括青少年型)。
表1. Ⅰ型與Ⅱ型OP的特點(diǎn)[1]
常見的骨質(zhì)疏松癥OP模型構(gòu)建方式:
關(guān)于OP的研究(發(fā)病機(jī)制、藥物篩選、防治手段等)都離不開動(dòng)物模型的構(gòu)建和應(yīng)用[2]。由于OP發(fā)病機(jī)制較為復(fù)雜、藥物作用機(jī)制與作用靶點(diǎn)不同,因此抗骨質(zhì)疏松癥藥物藥效學(xué)研究過(guò)程中動(dòng)物模型的選擇有所不同。
構(gòu)建骨質(zhì)疏松癥原則:
理想的OP模型至少需要符合以下幾點(diǎn)[3]:
一是簡(jiǎn)便,即建模方法簡(jiǎn)單,周期短,建模過(guò)程具有較強(qiáng)的可控性和可操作性;
二是經(jīng)濟(jì),即建模費(fèi)用適中,可大批量應(yīng)用;
三是相似性好,能較好地模擬OP發(fā)生和發(fā)展的過(guò)程。
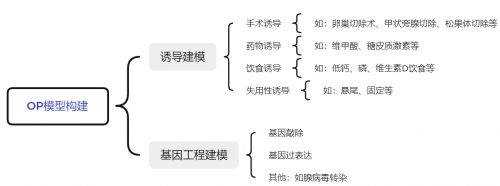
圖2. OP模型構(gòu)建方式
構(gòu)建骨質(zhì)疏松癥兩種方法:
經(jīng)過(guò)長(zhǎng)期實(shí)踐探索,OP 研究中模式動(dòng)物種類繁多,造模方法可概括為誘導(dǎo)建模和基因工程建模兩類。
1、誘導(dǎo)建模
誘導(dǎo)建模根據(jù)誘導(dǎo)原理和方式的不同可分為手術(shù)誘導(dǎo)https://www.gempharmatech.com/produce/model/10.html(卵巢切除術(shù)、甲狀旁腺切除、松果體切除等)、藥物誘導(dǎo)(如維甲酸、糖皮質(zhì)激素等)、飲食誘導(dǎo)(如低鈣、磷、維生素D飲食等)、失用性誘導(dǎo)(如懸尾、固定等)等。
2、基因工程建模
基因工程動(dòng)物https://www.gempharmatech.com/technology/customization.html主要包括基因敲除模型(全身性敲除、條件性敲除)、基因過(guò)表達(dá)模型以及腺病毒轉(zhuǎn)染等方式構(gòu)建的其他模型[4]。
集萃藥康OP模型資源-代繁骨質(zhì)疏松動(dòng)物模型小鼠品系種類:
集萃藥康深耕模式動(dòng)物領(lǐng)域多年,擁有豐富的模型構(gòu)建經(jīng)驗(yàn),并自主建立了腫瘤、代謝、自免、神經(jīng)等藥理藥效平臺(tái),可提供臨床前的體內(nèi)、外藥效評(píng)價(jià)服務(wù)。為助力骨質(zhì)疏松相關(guān)藥物研發(fā),集萃藥康通過(guò)基因編輯、手術(shù)誘導(dǎo)等方式構(gòu)建了多種骨質(zhì)疏松OP模型https://www.gempharmatech.com/produce/model/221.html,滿足不同藥物評(píng)價(jià)需求。
1、基因編輯的自發(fā)OP模型
人體骨組織處于不斷重建中,成骨細(xì)胞骨形成與破骨細(xì)胞骨吸收之間的聯(lián)系是骨代謝平衡的必要條件,而骨保護(hù)素(OPG)/核因子κβ受體活化因子(RANK)/核因子κβ受體活化因子配體(RANKL)信號(hào)通路是成骨細(xì)胞與破骨細(xì)胞之間通訊的重要橋梁[5]。
RANKL(TNFSF11)是TNF超家族成員,參與免疫調(diào)節(jié)及骨代謝(形成/吸收),是破骨細(xì)胞分化及成熟的重要激活因子。RANKL通過(guò)與RANK結(jié)合在調(diào)控破骨細(xì)胞的形成及其在骨重建中發(fā)揮重要作用。而OPG通過(guò)與RANKL結(jié)合,阻斷RANK與RANKL結(jié)合,從而抑制骨吸收,維持骨代謝平衡[5-6]。因此,過(guò)表達(dá)RANKL或下調(diào)OPG水平可能會(huì)導(dǎo)致破骨細(xì)胞過(guò)度活化而出現(xiàn)OP。
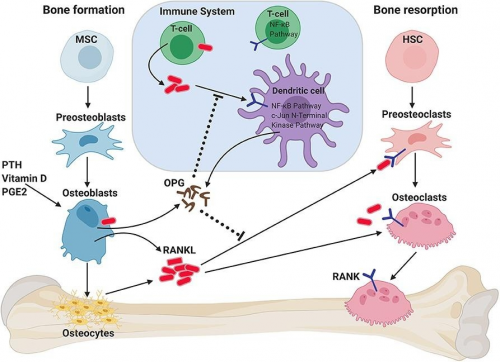
圖3. OPG/RANK/RANKL在骨穩(wěn)態(tài)中的作用[7]
OPG/RANK/RANKL信號(hào)系統(tǒng)除調(diào)節(jié)骨代謝平衡外,也參與細(xì)胞增殖、血管硬化、腫瘤骨轉(zhuǎn)移、炎癥和骨免疫等多種生理生化過(guò)程[8]。因此,靶向OPG、RANKL等靶點(diǎn)開發(fā)治療骨質(zhì)疏松及其他骨代謝疾病治療藥物具有重要意義。
集萃藥康采用BAC轉(zhuǎn)基因技術(shù)https://www.gempharmatech.com/produce/model/31.html制作了攜帶完整人類RANKL基因的B6-hRANKL轉(zhuǎn)基因小鼠模型https://www.gempharmatech.com/shop/detail/7411.html,可自發(fā)出現(xiàn)骨質(zhì)疏松癥狀。集萃藥康進(jìn)一步將B6-hRANKL-Tg轉(zhuǎn)基因小鼠與mOPG-KO小鼠配繁,獲得了B6-hRANKL-mOPG+/-模型,RANKL的過(guò)表達(dá)和OPG的下調(diào)使得該模型表現(xiàn)出更加嚴(yán)重的骨質(zhì)疏松表型,可用于評(píng)價(jià)靶向人RANKL的抗骨質(zhì)疏松藥物的療效。
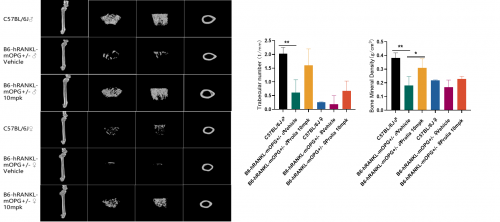
圖4. 基于B6-hRANKL-mOPG+/-小鼠的體內(nèi)藥效試驗(yàn)
Micro CT影像圖結(jié)果顯示:與野生型小鼠相比,B6-hRANKL-mOPG+/-小鼠的骨小梁數(shù)量減少,骨密度降低,抗人類RANKL抗體(Prolia / Denosumab)干預(yù)后,B6-hRANKL-mOPG+/-小鼠的骨小梁數(shù)量增多,骨密度增高,表型得到很好改善。
2、去卵巢法構(gòu)建OP模型
去卵巢造模法是將適齡雌鼠通過(guò)手術(shù)去勢(shì),用于模擬人類女性絕經(jīng)后雌激素水平降低引發(fā)的骨質(zhì)疏松。雌激素是維持骨代謝平衡的重要物質(zhì)之一,可通過(guò)OPG/RANK/RANKL途徑直接作用于破骨細(xì)胞,促使破骨細(xì)胞凋亡、抑制破骨細(xì)胞分化、成熟,從而使骨吸收減少[9]。另外,雌激素通過(guò)改變轉(zhuǎn)錄因子的活性,調(diào)節(jié)自噬,減弱氧化應(yīng)激反應(yīng),降低核因子κB(nuclear factor kappa-B,NF-κB)活性,降低骨硬化蛋白,抑制成骨細(xì)胞凋亡并增加成骨細(xì)胞的存活時(shí)間,從而影響骨代謝。因此雌激素缺乏可引起骨代謝失衡,導(dǎo)致骨量減少或骨質(zhì)疏松[10]。去卵巢造模法可以降低雌鼠體內(nèi)雌激素水平,模擬女性絕經(jīng)后骨質(zhì)疏松。一般,將小鼠卵巢摘除后正常飲食8~12周,即可建立骨質(zhì)疏松模型。
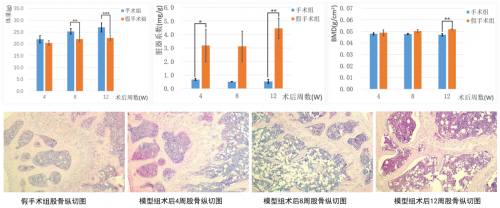
圖5. 卵巢切除的小鼠OP模型表型觀察
12周雌鼠摘除卵巢12周后的體重明顯高于假手術(shù)組,小鼠卵巢摘除后子宮的臟器系數(shù)顯著降低,骨密度顯著降低。取小鼠股骨進(jìn)行HE染色,結(jié)果顯示模型組相比于假手術(shù)組,大體上股骨骨組織的骨小梁邊緣粗糙,骨小梁間隙增大,骨小梁排列不齊且有斷點(diǎn),骨髓腔內(nèi)空泡增多。
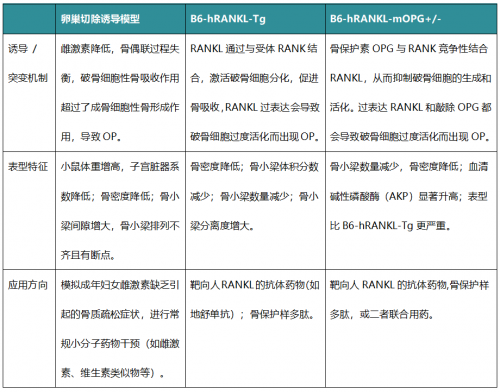
OP模型比較
參考文獻(xiàn):
李險(xiǎn)峰. 骨質(zhì)疏松癥的分類和分型. 中國(guó)全科醫(yī)學(xué). 2005, (16).
薛麗香, 張鳳珠, 孫瑞娟, 等. 我國(guó)疾病動(dòng)物模型的研究現(xiàn)狀和展望. 中國(guó)科學(xué): 生命科學(xué), 2014, 44(9) : 851-861.
孫凱, 魏戌, 朱立國(guó), 等. 病證結(jié)合模式下骨質(zhì)疏松癥實(shí)驗(yàn)動(dòng)物模型的研究進(jìn)展. 中國(guó)骨質(zhì)疏松雜志, 2019, 25 ( 9) :1340-1344.
江瑞雪, 蔣欣泉, 文晉. 骨質(zhì)疏松動(dòng)物模型研究現(xiàn)狀與進(jìn)展. 中國(guó)骨質(zhì)疏松雜志. 2022, 28(07).
李小娜. OPG/RANK/RANKL信號(hào)通路研究進(jìn)展.河南醫(yī)學(xué)研究, 2014.
Rinotas, Vagelis, et al. Novel genetic models of osteoporosis by overexpression of human RANKL in transgenic mice. Journal of Bone and Mineral Research 29.5 (2014): 1158-1169.
Jie Ming, Shane J F Cronin, Josef M Penninger. Targeting the RANKL/RANK/OPG Axis for Cancer Therapy. Front Oncol. 2020 Aug 7;10:1283.
屈曉龍, 蔣濤. OPG-RANKL-RANK信號(hào)系統(tǒng)與骨質(zhì)疏松治療的研究進(jìn)展. 生命科學(xué). 2018, 30(07).
Hadji P, Colli E, Regidor PA. Bone health in estrogen-free contraception[J]. Osteoporos Int, 2019, 30(12): 2391-2400.
Gavali S, Gupta MK, Daswani B, et al. Estrogen enhances human osteoblast survival and function via promotion of autophagy. Biochim Biophys Acta Mol Cell Res, 2019, 1866(9): 1498-1507.
本文地址:http://www.dayishuiji.com/jiankang/40434.html - 轉(zhuǎn)載請(qǐng)保留原文鏈接。| 免責(zé)聲明:本文轉(zhuǎn)載上述內(nèi)容出于傳遞更多信息之目的,不代表本網(wǎng)的觀點(diǎn)和立場(chǎng),故本網(wǎng)對(duì)其真實(shí)性不負(fù)責(zé),也不構(gòu)成任何其他建議;本網(wǎng)站圖片,文字之類版權(quán)申明,因?yàn)榫W(wǎng)站可以由注冊(cè)用戶自行上傳圖片或文字,本網(wǎng)站無(wú)法鑒別所上傳圖片或文字的知識(shí)版權(quán),如果侵犯,請(qǐng)及時(shí)通知我們,本網(wǎng)站將在第一時(shí)間及時(shí)刪除。 |